DOI: 10.1002/adfm.202007440
由创伤、器官扩张或压迫引起的疏松软组织的无创修复尚未得到妥善解决。本文提出了一种制备热收缩电纺纤维带(HS-EFT)的新方法,其中聚乳酸-羟基乙酸(HS-EFT)的收缩使疏松的筋膜在体温下向后拉,同时收缩的机械力转化为一个外部信号来调节成纤维细胞的行为。由于它在五天内收缩了40%以上,因此观察到成纤维细胞在收缩的纤维膜上快速增殖,随后形成更多的应力纤维,从而促进了机械刺激敏感的共转录分子,即yes相关蛋白(YAP)的核转移,最终使新的细胞外基质(ECM)沉积并且使组织得到强化。此外,在修复兔筋膜缺损的过程中,纤维带将疏松组织聚集在一起,最终缩小了伤口面积,并进行了组织修复。因此,HS-EFT技术为无创重建疏松软组织提供了有益的启示。
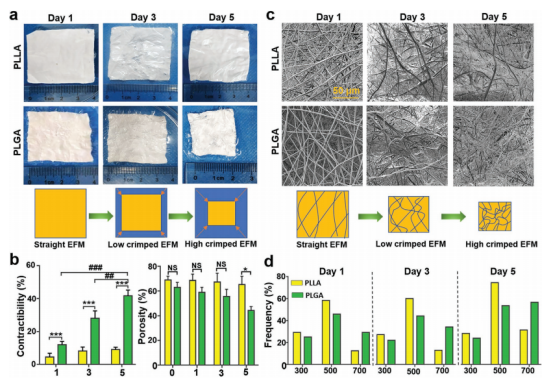
图1.静电纺丝纳米纤维的收缩特性评估。a)PLGA EFM在37℃ PBS中五天内显著收缩,而对照PLLA几乎未观察到收缩。b)收缩前后电纺纤维膜的SEM图像。c)不同时间点的EFM的收缩率和孔隙率数据。d)收缩前后EFM的纤维直径定量。
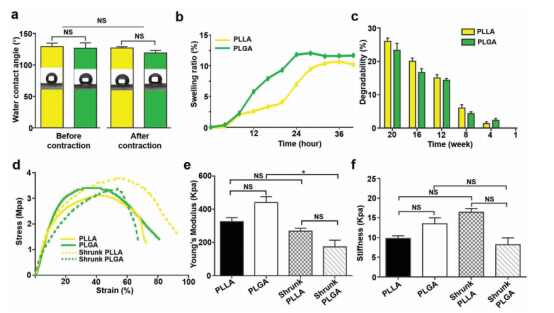
图2.EFT的表征。a)收缩前后纤维垫的水接触角。b,c)PLLA和PLGA EFM在不同时间点的溶胀率和降解特性。d-f)收缩前后EFM的应力-应变研究以及杨氏模量和刚度的量化。
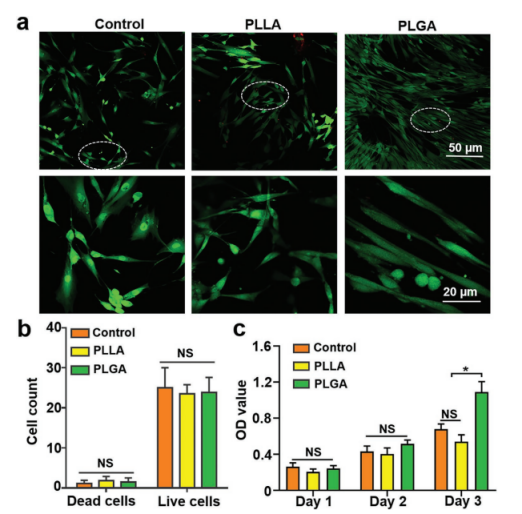
图3.体外生物相容性研究。a)第三天EFM的活/死荧光结果。b)对照、PLLA、PLGA组的活细胞计数。c)不同组的CCK-8定量结果,分别为期1天、2天和3天。
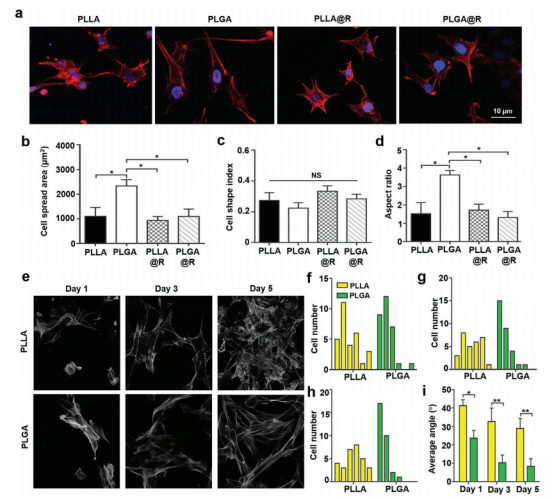
图4.体外细胞形态研究。a)在带有或不带钢环的PLLA和PLGA纤维EFMs上HFVs的细胞骨架染色。b)在带有或不带钢环的EFMs上对单个细胞扩散区域的量化。c,d)在带有或不带钢环的EFMs上30个单HVFs的细胞形态指数和纵横比。e)HVF在PLLA和PLGA EFMs上的肌动蛋白比对。f-h)在第1天、第3天和第5天对肌动蛋白纤维的平均角度和细胞长轴进行定量。i)肌动蛋白纤维细胞轴角在不同时间点的统计。
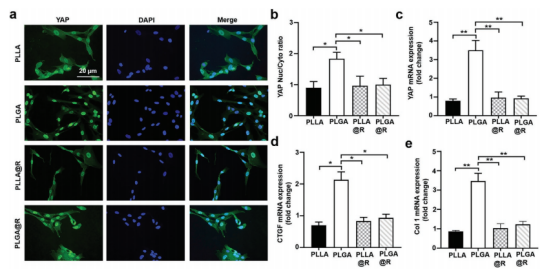
图5.纤维回缩力的机械传导和YAP的核转移。a)在带有或不带钢环的EFMs上HVFs中YAP的免疫组织化学染色图像。细胞用YAP染成绿色,细胞核用DAPI染成蓝色。b)在第3天对HVFs中的平均YAP核/胞质比率进行定量。c-e)在带有或不带钢环的EFMs上HVFs中YAP、CTGF和Col1的mRNA水平。
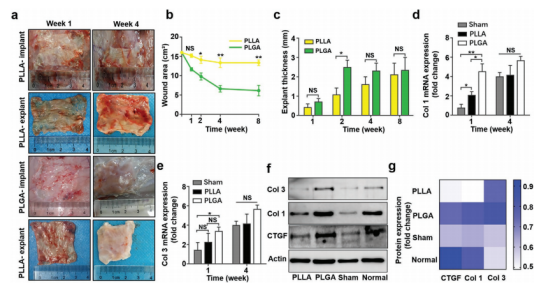
图6.疏松软组织修复的体内研究。a)第1周和第4周PLLA和PLGA EFT植入物和外植体的代表性照片。b)每个时间点不同组的伤口面积。c)每个时间点不同组的外植体厚度。d,e)用PLLA和PLGA EFTs处理兔腹壁缺损后,Col1、Col3的相对mRNA表达。f,g)蛋白质印迹结果以检测Col1、Col3和CTGF的表达以及每组蛋白质表达的定量。
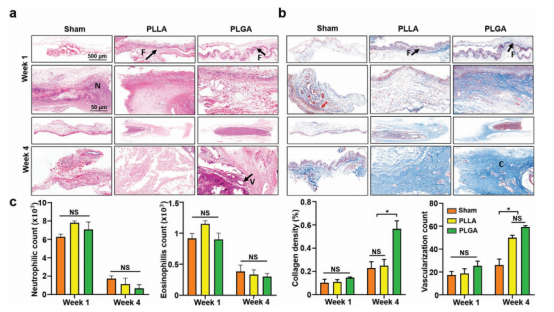
图7.PLLA、PLGA和假手术组伤口修复的组织学分析。a)第1周和第4周PLLA、PLGA和假手术组中筋膜组织的HE染色切片(上图:横截面;下图:纵切面)(F,N,V分别代表纤维、中性粒细胞和血管)。b)第1周和第4周每组筋膜组织的Masson染色切片(上图:横截面;下图:纵切面)(F,C分别代表纤维和胶原蛋白)。c)在第1周和第4周对嗜中性细胞、嗜酸性细胞、胶原蛋白沉积和新血管形成进行定量。
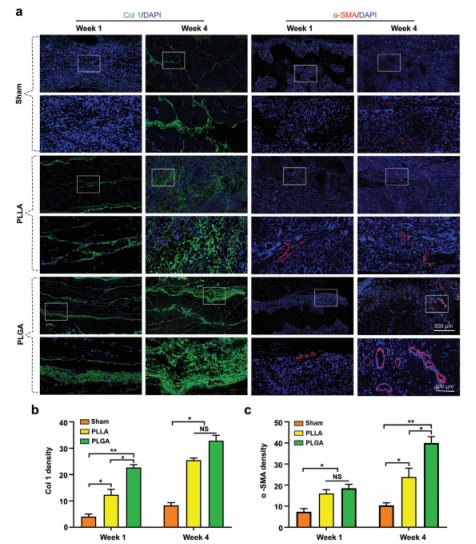
图8.假手术、PLLA和PLGA组中Col1和α-SMA的免疫荧光染色。a)在第一周和第四周对Col1和α-SMA进行免疫组织化学染色的图像。b,c)在第一周和第四周对Col1和α-SMA的免疫荧光强度进行定量。
